- Fase preliminare: messa a punto delle metodiche
Nella fase preliminare, in scala di laboratorio, sono stati lavorati, in batch, lotti di 500 g di lenticchie, sottoposte a decorticatura per sbattimento meccanico per mezzo di un mixer da laboratorio, ottenendo circa 65 g di cuticola. La cuticola è stata separata con l’utilizzo di vibrovaglio, e la cuticola con granulometria polverosa è stata scartata per evitare eccessivo intorbidimento in fase di preparazione dei campioni da sottoporre all’estrazione. Dopo un’approfondita ricerca bibliografica, facendo riferimento alle procedure riportate da Zhang et al. (2015) sono state messe a punto:
- la procedura di estrazione;
- le procedure per la determinazione, attraverso saggi spettrofotometrici, della componente fenolica totale (total phenolic content TPC), del contenuto totale dei flavonoidi (total flavonoids content TFC) e del contenuto dei tannini condensati (condensed tannin content CTC).
Facendo riferimento alla procedura riportata da Zhang et al. (2015), è stato definito il protocollo di estrazione che ha consentito la massima estrazione di TPC, TFC e CTC dalla cuticola di lenticchie. Nello specifico si tratta di un’estrazione solido-liquido di 0,2 g di cuticole di lenticchie in 40 ml di una soluzione acquosa di metanolo al 70% acidificata con lo 0,1% di HCl, in tre fasi di estrazioni da 15 ore, con volumi rispettivamente di 20 ml, 10 ml e 10 ml, in agitazione continua e a temperatura ambiente. Sull’estratto metanolico totale, ovvero l’insieme delle tre frazioni di estrazione con volume finale di 40 ml, sono stati eseguiti i saggi spettrofotometrici per la determinazione e quantificazione dei TPC, TFC e CTC. Al fine di confermare quanto riportato in letteratura, ovvero che le cuticole delle lenticchie sono ricche in polifenoli, tannini e flavonoli (Dueñas et al., 2003), sono state eseguite prove di estrazione su campioni di lenticchia intera, polpa e cuticole e sugli estratti totali sono stati eseguiti i saggi spettrofotometrici TPC, TFC, CTC. Come è possibile osservare dalla Fig.1, i dati ottenuti sono in accordo con quanto riportato in letteratura.

Valutando quelli che potrebbero essere gli effetti indesiderati dovuti alla presenza del metanolo nei mangimi da fornire ai bovini, è stata vagliata successivamente la possibilità di utilizzare solventi differenti:
- soluzione acquosa acidificata (0,1% di HCl)
- soluzione etanolica al 40% acidificata (0,1% HCl)
- soluzione etanolica al 60% acidificata (0,1% HCl)
- soluzione metanolica al 70% acidificata (0,1% HCl)
Nel grafico sottostante (Fig. 2) sono riportate le percentuali di estrazione delle diverse componenti (TPC, TFC, CTC), calcolate in relazione all’estrazione con metanolo considerata, fino a questo momento, l’optimum. La percentuale di estrazione ottenibile con la soluzione etanolica al 60% acidificata corrisponde al 96 % dei TPC, al 70% dei TFC e all’86,5% dei CTC estraibili mediante l’impiego della soluzione metanolica al 70% acidificata.
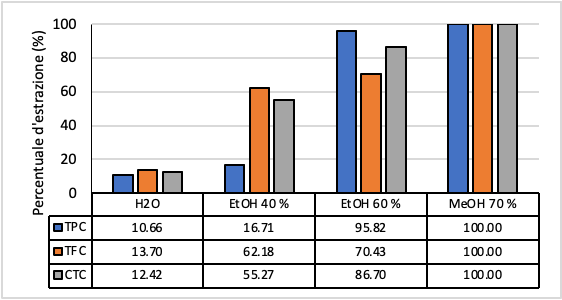
Avendo appurato che la soluzione etanolica al 60% acidificata potrebbe essere utilizzata in alternativa alla soluzione metanolica al 70% acidificata, si è cercato di ottimizzare il processo di estrazione vagliando sia la possibilità di utilizzare il trattamento delle microonde che quello degli ultrasuoni. Il trattamento effettuato con le microonde è stato successivamente scartato poiché venivano raggiunte temperature elevate che provocavano perdita di solvente. Ci si è concentrati quindi sulla possibilità di utilizzare gli ultrasuoni per aumentare la capacità estrattiva dell’etanolo. Gli estratti analizzati sono stati:
- Etanolo 60% acidificato con trattamento ad ultrasuoni di 4 ore;
- Etanolo 60% acidificato con trattamento ad ultrasuoni di 11 ore;
Tali estratti sono stati confrontati con quelli ottenuti mediante l’utilizzo di soluzione MeOH al 70% ed EtOH al 60% in tre fasi di estrazioni da 15 ore senza trattamento coadiuvante. Dai dati riportati in Fig. 3, si evince come prolungando il tempo del trattamento ad ultrasuoni da 4 a 11 ore si estrae circa il 10-15% in più. Valori più elevati potrebbero essere ottenuti aumentando la durata del trattamento con gli ultrasuoni.
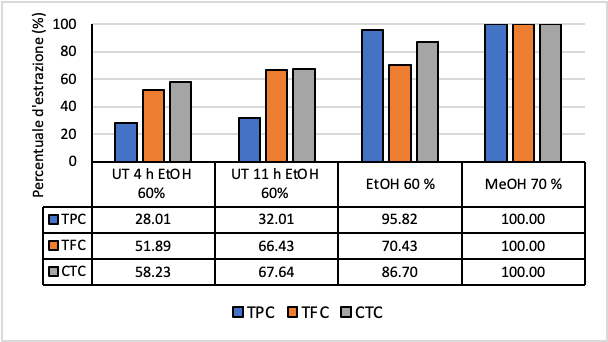
- Valutazione della sostituzione del solvente metanolo con l’etanolo nell’estrazione di composti attivi da tegumenti ottenuti mediante l’impiego della decorticatrice.
Durante il mese di dicembre, grazie alla messa a punto del sistema di decorticazione, è stato possibile sottoporre alle analisi direttamente lo scarto ottenuto mediante tale processo. È stata quindi confrontata la capacità estrattiva della soluzione metanolica al 70% acidificata con quella della soluzione etanolica al 60% acidificata sui nuovi campioni e, come riportato in Fig. 4, la sostituzione del metanolo con l’etanolo provoca riduzioni lievi, seppur significative (p<0,05) solo per quanto concerne il CTC nell’estratto.

- Riduzione dei volumi di solvente
Sono state condotte successivamente prove per valutare la possibilità di ridurre il rapporto solvente:tegumento al fine di migliorare l’efficienza del processo di estrazione dei composti di nostro interesse. Nel dettaglio, 0,2 g di cuticola di lenticchia, ottenuta mediante l’impiego della decorticatrice messa a punto, sono stati estratti con 40, 30, 20 ml totali di una soluzione etanolica al 60% acidificata in tre tempi da 15 h l’uno. Il volume totale di 40, 30 e 20 ml è stato ottenuto sommando le diverse aliquote di solvente aggiunte durante i tre tempi di estrazione (Tab. 1).
Tabella 1. Volume di solvente totale e diviso nelle tre estrazioni utilizzato per ottenere i composti fenolici dalle cuticole di lenticchie.
| Estrazione | C 1 | C 2 | C 3 |
| I (volume ml) | 20 | 15 | 10 |
| II (volume ml) | 10 | 7,5 | 5 |
| III (volume ml) | 10 | 7,5 | 5 |
| Volume totale (ml) | 40 | 30 | 20 |
Per i 3 volumi di estrazione è stata valutata la concentrazione totale di TPC, TFC e CTC. Come riportato in Fig. 5, riducendo il volume di estrazione da 40 a 20 ml ci sono delle differenze che, seppur minime, risultano essere significative (p<0,05). Tale risultato andrebbe valutato in relazione all’efficienza economica del processo tenendo conto delle elevate quantità di estratto che andrebbero prodotte al fine di produrre le microcapsule.

È stato inoltre valutato dettagliatamente anche il contributo specifico delle tre diverse estrazioni, sul quantitativo totale di tannini condensati (CTC) (Fig. 6) e la percentuale relativa di estrazione, rispetto al primo tempo, della seconda e della terza estrazione (Tab. 2). Come si evince dalla Fig. 6, la riduzione del volume finale di solvente ha un effetto minimo, seppur significativo, sul quantitativo di tannini estratti nei tre diversi tempi. Inoltre, come è possibile osservare dalla Tabella 3, la riduzione del volume di solvente influenza positivamente la capacità estrattiva nelle tre frazioni.

Tabella 2. Percentuale di estrazione ottenuta nei tre tempi.
| Estrazione | C 1 | C 2 | C 3 |
| Volume finale 40 ml | Volume finale 30 ml | Volume finale 20 ml | |
| I (%) | 100 | 100 | 100 |
| II (%) | 10,6 | 13,4 | 21,9 |
| III (%) | 5,32 | 8,74 | 18,14 |
Valutazione della sostituzione del solvente etanolo con l’acqua nell’estrazione di composti attivi da tegumenti ottenuti mediante l’impiego della decorticatrice
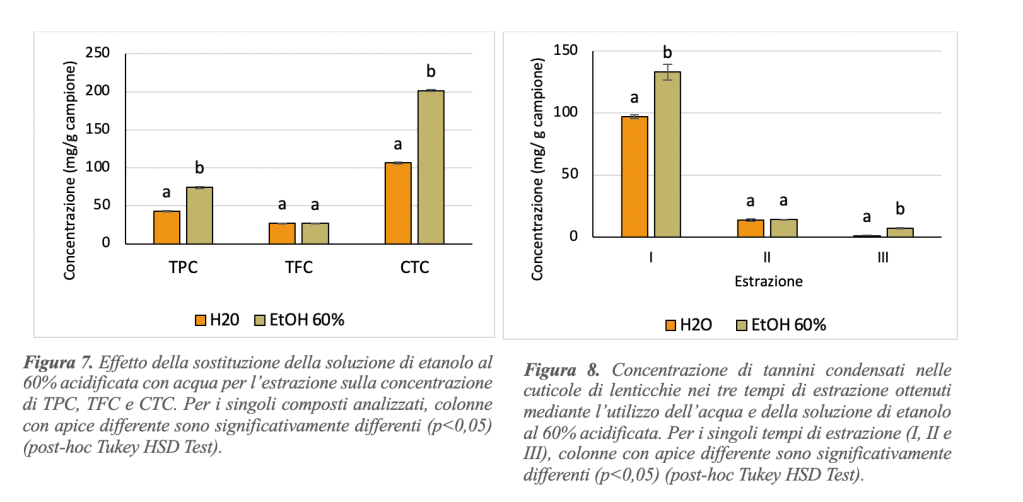
Nell’ottica di ottimizzare la sostenibilità del processo di estrazione è stata valutata la possibilità di estrarre i TPC, i TFC e i CTC in acqua. Si è proceduto dunque all’estrazione, considerando un rapporto solvente:tegumento di 40:0,2 in tre estrazioni da 15 h l’una a temperatura ambiente. In Fig. 7 è stato riportato il confronto tra la concentrazione di TPC, TFC e CTC ottenuta utilizzando l’acqua come solvente di estrazione in alternativa alla soluzione di etanolo al 60% acidificata considerata come l’optimum. Impiegando l’acqua a temperatura ambiente come solvente, si è estratto il 57,63% di TPC, il 100% di TFC ed il 52,74% di CTC rispetto a quanto è possibile ottenere utilizzando una soluzione di etanolo al 60% acidificata. Andando a valutare la concentrazione di composti attivi ottenibili nei tre tempi delle estrazioni è possibile vedere che utilizzando la sola acqua, la terza frazione non sembrerebbe indispensabile (Fig. 8).
- Valutazione dell’incremento della temperatura di estrazione sul contenuto di TPC, TFC e CTC
Per aumentare il quantitativo di composti attivi estratti utilizzando l’acqua in qualità di solvente, si è andati ad agire sulla temperatura. Purtroppo, l’aumento della temperatura di estrazione a 50 °C non ha portato ad un incremento significativo dei composti attivi estratti. Per i TPC e per i CTC si è osservata addirittura una riduzione imputabile, probabilmente, alla diversa modalità di agitazione dei campioni, condizione contingente all’utilizzo di temperature più elevate (Fig. 9).

Come riportato in letteratura, un aumento significativo della concentrazione di composti attivi estraibili con acqua dalle cuticole di lenticchie potrebbe essere ottenuto innalzando ulteriormente la temperatura, Kratchanova et al., (2010) riportano una temperatura di ben 90°C, mediante l’acidificazione dell’acqua con HCl 12 N (Cheaib et al., 2018) o mediante l’impiego degli ultrasuoni (Pingret et al., 2012).
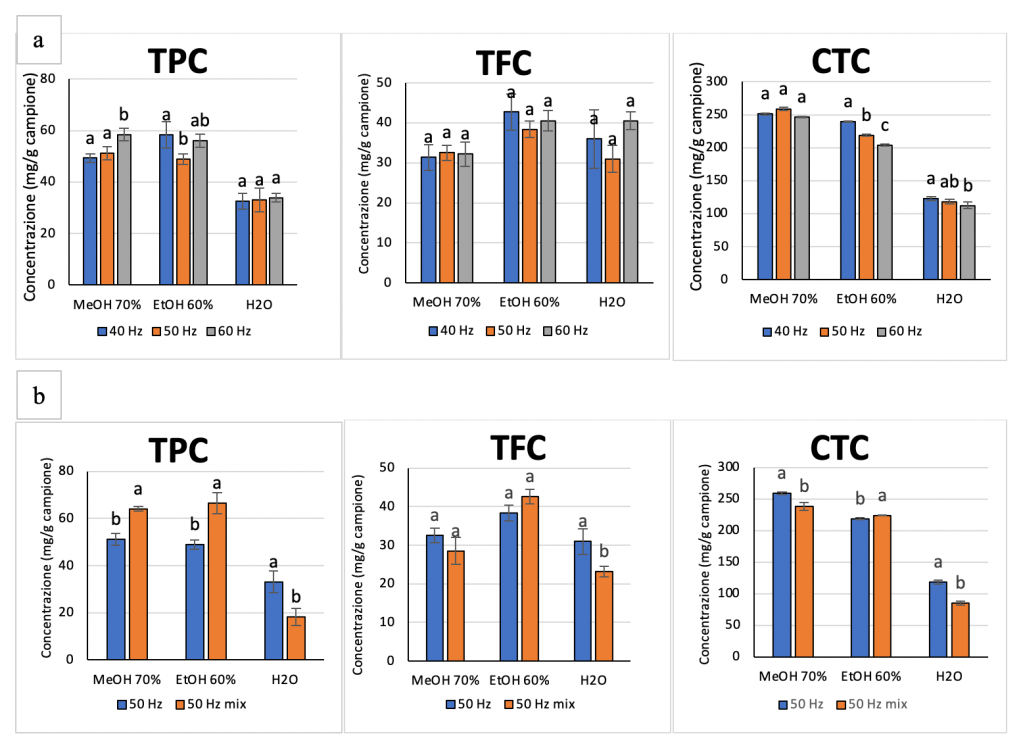
Si è proceduto quindi ad indagare se, un diverso settaggio della frequenza della decorticatrice (40-50-60 Hz) potesse avere degli effetti significativi sull’estrazione di TPC, TFC e CTC utilizzando tre diversi solventi di estrazione: soluzione metanolica al 70% acidificata, soluzione etanolica al 60% acidificata e acqua acidificata. Come è possibile evincere dalla Fig.10(a), utilizzando l’acqua come solvente di estrazione, che sarebbe la scelta ovviamente più sostenibile, si può concludere che la diversa frequenza settata nella decorticatrice, non ha effetti significativi sull’estrazione dei composti bioattivi. Si è proceduto quindi ad indagare se l’aumento della superficie di contatto tra le cuticole ed il solvente, ottenibile attraverso uno step aggiuntivo di triturazione e setacciatura (< 200 mm) delle cuticole stesse, potesse aumentare considerevolmente il contenuto di TPC, TFC e CTC nell’estratto. Come mostrato nella Fig. 10(b), sebbene ci sia un incremento significativo dell’estrazione di composti bioattivi utilizzando sia la soluzione metanolica al 70%, che soluzione etanolica al 60% e l’acqua acidificata, tale risultato non giustificherebbe l’aggiunta di uno step successivo a quello della decorticazione.
- Monitoraggio della variazione della concentrazione di TPC, TFC e CTC durante le 15 h di estrazione
Durante la fase iniziale di sperimentazione è stata appurata la necessità di effettuare tre estrazioni successive sulla cuticola di lenticchia della durata singola di 15 h, poiché ognuna di esse contribuiva significativamente all’estrazione di TPC, TFC e CTC. Obiettivo di quest’ultima fase di analisi è stato il monitoraggio, con prelievi effettuati ogni 2 h, di tutte e tre le estrazioni dalla durata singola di 15 ore. A titolo d’esempio, in Fig. 11 è stato riportato l’andamento della concentrazione estratta di TPC, TFC e CTC durante le 15 ore della prima estrazione utilizzando etanolo al 60% acidificato e acqua acidificata come solventi di estrazione. Come è possibile osservare dopo un certo numero di ore di estrazione viene raggiunto un plateau e, per tale motivo, le 15 ore di estrazione potrebbero essere ridotte. Nello specifico, per quanto riguarda la prima fase di estrazione questa potrebbe essere ridotta da 15 h a 12 per entrambi i solventi valutati. La seconda fase di estrazione potrebbe essere invece ridotta a 8 h considerando l’acqua come solvente di estrazione e a 12 h considerando invece l’etanolo. La terza fase sembrerebbe non necessaria quando si utilizza l’acqua come solvente mentre potrebbe essere ridotta a 8 h utilizzando l’etanolo.

Confronto tra le metodologie estrattive proposte
Successivamente è stata comparata l’estrazione in acqua acidulata (pH 3,1) con o senza l’impiego di ultrasuoni. I protocolli operativi sono stati progettati in collaborazione tra le unità di ricerca AGR09 e AGR15. Dai risultati delle analisi risulta che il tempo ottimale di trattamento è intorno alle 2 ore, con un’estrazione di ca. 155 mg/g.
Ciononostante con l’estrazione in soluzione acquosa acidificata senza il supporto della tecnologia a US, a dispetto dei lunghi tempi di estrazione, sono stati raggiunti i risultati migliori sulla frazione tanninica come è possibile osservare dalla Figura 12, in cui è stata riportata la quantità di tannini estratta, utilizzando acqua acidificata, metanolo al 70%, etanolo al 60% mediante l’impiego del protocollo proposto da Zhang et al. (2015) che consisteva in tre fasi di estrazioni da 15 h e l’estrazione in acqua acidificata abbinata a diversi trattamenti US.
I valori di confronto per l’estrazione con solvente chimico nelle massime condizioni di estrazione possibili adottate nel laboratorio dell’unità AGR15 sono risultati pari a 293 mg/g. I valori ottenuti con tecnologie “green” sono in linea con i valori riportati da vari autori per l’estrazione di tannini ed altri composti da matrici vegetali. Inoltre, la limitazione delle rese di estrazione dei composti fenolici in conseguenza dell’impossibilità di utilizzare solventi chimici, era stato evidenziato anche tra i punti di debolezza della proposta progettuale. Il contributo all’estrazione della tecnica ad ultrasuoni, nelle condizioni testate, non è stato soddisfacente. Infatti, come è possibile osservare dalla Figura 12, in cui le diverse metodologie di estrazione sono state confrontate, non si evidenzia un vantaggio significativo nell’estrazione quando all’estrazione con il solvente acqua è stato aggiunto l’effetto degli ultrasuoni. Rimarrebbe, peraltro, un problema tuttora irrisolto a livello industriale, cioè la scalabilità dell’estrazione a ultrasuoni dal livello di laboratorio a quello industriale.

In riferimento agli obiettivi generali e specifici del progetto, dunque, dal confronto tra le tecnologie estrattive proposte, e dall’analisi dei dati relativi alla quantità di tannini estratti, risulta che il metodo migliore per la formulazione di estratti da avviare alla trasformazione per la produzione di un integratore per la dieta delle bovine è l’estrazione in acqua acidifcata.
Appare ovvio che, anche dal punto di vista energetico e di impatto ambientale, questa risulta la tecnica migliore. Infatti, una
linea completa per la produzione di estratto da cuticola di lenticchia dovrebbe prevedere i seguenti elementi impiantistici: un serbatoio polmone per il solvente (acqua), un tank per la estrazione solido/liquido, con possibilità di gestione della temperatura di riscaldamento e raffreddamento a mezzo di soluzione circolante nell’intercapedine del tank, munito di sonde di controllo pH e sistema di gestione del pH (per utilizzo con acqua acidulata), un sistema di ricircolo del solvente per un parziale rinfresco, periodicamente, del solvente. A fine trattamento, il solvente, separato dalla massa solida esausta, viene alimentato, dopo un parziale allontanamento dell’acqua per mezzo di un concentratore a bassa pressione (T evaporazione max 50°C), e alimentato all’impianto per la microincapsulazione.
Caratterizzazione dell’estratto in acqua
L’estratto tannico è stato idrolizzato con HCl (concentrazione finale 2 N) e riscaldato a 85 °C per 1 ora. I campioni sono stati lasciati raffreddare a temperatura ambiente e quindi centrifugati a 3000 g per 5 min. Il supernatante è stato filtrato e sottoposto ad analisi HPLC. In Figura 13 è stata riportata l’identificazione dei composti fenolici presenti nell’estratto.

