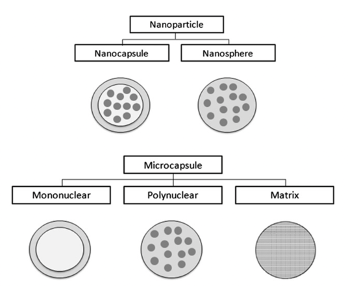
L’ incapsulazione può essere definita come una tecnologia che prevede l’inclusione di ingredienti bioattivi sensibili, siano essi solidi, liquidi o gassosi, all’interno di una o più matrici polimeriche protettive. La tecnica è attualmente impiegata nel settore farmaceutico, chimico, medico e biotecnologico in quanto offre la possibilità di migliorare le proprietà funzionali di un determinato composto. Si è affermata anche nel campo alimentare, soprattutto negli ultimi decenni, ovvero da quando l’alimentazione è passata dall’essere un mero strumento di soddisfacimento dei bisogni a mezzo per la promozione del benessere psico-fisico e delle patologie cronico-degenerative. L’incapsulazione si basa sul rivestimento di un composto attivo (core) con uno o più materiali di copertura (shell). Il core è il composto da incapsulare, ovvero il principio attivo, detto anche nucleo o fase interna; può avere una forma sferica o irregolare e può essere composto da uno o più ingredienti sotto forma di goccioline liquide, particelle solide o bolle di gas. Lo shell, definito anche rivestimento, wall, membrana, involucro o materiale di parete, può essere a singolo o doppio strato (Poshadri e Aparna, 2010). In base alle dimensioni della capsula, il nome e la tecnologia dell’incapsulazione cambiano (Tolve et al., 2016). Si può parlare, infatti, sia di nanoincapsulazione che di microincapsulazione: dalla prima si possono ottenere oltre alle nanocapsule, ossia sistemi vescicolari in cui il composto bioattivo è circondato da una membrana polimerica unica, anche le nanosfere, ossia sistemi a matrice in cui il composto bioattivo è uniformemente disperso. Dalla microincapsulazione si ottengono microcapsule o microsfere con dimensioni che variano da 3 a 800 μm (Fig. 1).
Tra le diverse tipologie, la microincapsulazione è l’applicazione più comune in ambito alimentare. La tecnologia della microincapsulazione nasce a cavallo tra anni ’20 -‘30 anche se da un punto di vista industriale il primo vero successo è datato 1955, quando al National Cash Register Company (NCR), di Dayton Ohio, venne brevettato un processo di coacervazione della gelatina in grado di incapsulare un pigmento: era nata la carta “autocopiante” che si usa tuttora, diversa dalla vecchia carta carbone che utilizzava inchiostro secco e cera. Dagli anni 50 ad oggi è avvenuto un continuo e crescente sviluppo della tecnologia, tuttora ampiamente diffusa in un gran numero di settori industriali.
A seconda della natura del principio attivo e del materiale di rivestimento utilizzato, le microcapsule possono essere classificate in mononucleari, polinucleari o a matrice. Le microcapsule mononucleari (core-shell) sono caratterizzate da un guscio che racchiude un solo nucleo; le polinucleari hanno, così come indica il nome, molti nuclei racchiusi all’interno del guscio; nei tipi a matrice, invece, il materiale del nucleo è distribuito omogeneamente nel materiale di rivestimento (Tolve et al., 2016).
Oltre alla forma sferica, le microcapsule possono assumere anche forma irregolare, così come mostrato in Figura 2.

Nella microincapsulazione in matrici protettive la scelta del materiale incapsulante, ovvero del polimero di rivestimento, è essenziale per la buona riuscita del processo. In base alla destinazione d’uso, possono essere selezionati polimeri di rivestimento particolari tali da conferire caratteristiche differenti alla microcapsula: si possono ottenere microcapsule resistenti agli agenti esterni oppure sensibili ad attrito, pressione, umidità o calore. I polimeri più comunemente utilizzati possono essere di origine naturale o sintetica ed è anche possibile l’impiego di materiali biodegradabili. La scelta dipende dal tipo di core che deve essere incapsulato, dalla tecnologia utilizzata, dall’uso e dall’applicazione finale a cui la microcapsula è destinata. Lo shell, ovvero il polimero di rivestimento, deve essere, in ogni caso, stabile nel tempo e deve essere permeabile o impermeabile, a seconda della destinazione. Necessariamente in ambito alimentare il rivestimento dovrà essere un polimero GRAS, ovvero Generally Recognized As Safe, ed inoltre dovrà essere:
- facile da lavorare e meccanicamente resistente;
- in grado di rivestire l’ingrediente attivo senza interagire con esso, sia durante il processo sia durante lo stoccaggio a lungo termine;
- in grado di non rilasciare impurità o altri residui;
- non tossico;
- protettivo nei confronti del materiale attivo soprattutto in determinate condizioni ambientali (ossigeno, calore, luce, umidità ecc.);
- capace di dissolversi e rilasciare il core in condizioni desiderate (Temiz e Ozturk, 2018).
Un unico materiale difficilmente possiede tutte queste proprietà e proprio per tale motivo può essere prevista la combinazione di sostanze differenti. Tra i materiali più utilizzati, in campo alimentare troviamo i carboidrati, le gomme, i lipidi e le proteine (Silva et al., 2014). Alcuni esempi sono riportati in Tabella 1.
Tabella 1. Tipologie di materiali di rivestimento utilizzati nella microincapsulazione alimentare (Poshadri e Aparna, 2010)

A seconda del tipo di rivestimento selezionato, le microcapsule ottenute saranno caratterizzate, tra l’altro, da una differente velocità di rilascio del core e da meccanismi di reattività, con l’ambiente circostante, completamente diversi. Per la microincapsulazione di additivi alimentari vengono spesso impiegati i carboidrati: amido, maltodestrina e sciroppo di glucosio sono tra le tipologie maggiormente usate poiché tra le più economiche. Tali polimeri sono caratterizzati da una bassa viscosità anche ad alte concentrazioni; tuttavia, a causa della quasi totale mancanza di proprietà emulsionanti, si preferisce usarli in combinazione con proteine, piuttosto che da sole (Dziezak, 1988). Le proteine, infatti, sono ottimi materiali di rivestimento per i processi di microincapsulazione soprattutto grazie alle loro proprietà funzionali, quali quella emulsionante, l’elevata solubilità, la bassa viscosità e la capacità di formare film. Tra le gomme, invece, la più comune è la gomma arabica per le proprietà emulsionanti e per la capacità di ritenzione delle componenti volatili. La gomma arabica è stata ampiamente utilizzata per la microincapsulazione di oli essenziali, polifenoli, aromi, sostanze coloranti naturali (oleoresine e carotenoidi), vitamine, batteri e probiotici (Mosawi e Thevenet, 2012). Molto utilizzato come polimero di rivestimento è anche l’alginato, un composto chimico estratto dalle pareti cellulari di alcune alghe. Presenta un’alta stabilità meccanica e permette di creare film molto sottili; di contro è molto sensibile all’acidità e, per questo, non viene utilizzato per la formulazione di microcapsule destinate a resistere ai succhi gastrici presenti nello stomaco. È preferito per la microincapsulazione di cellule microbiche, enzimi, ormoni, farmaci e oli, spesso in combinazione ad altri polimeri (Chan et al., 2009). La protezione fornita dal rivestimento ovviamente non è destinata a durare all’infinito. L’obiettivo è quello di proteggere l’ingrediente e successivamente rilasciarlo in modo che possa svolgere la funzione prevista (Putnam e Garret, 2005).
Per soddisfare le richieste diverse devono essere effettuate svariate prove di microincapsulazione, con differenti formulazioni e diverse proporzioni, fino ad ottenere i risultati desiderati.
La cinetica di rilascio del core obbedisce all’equazione:
𝑄=𝑣𝑡
dove Q è la quantità̀ di core rilasciato per unità di area di superficie esposta nel tempo t e v è la velocità di rilascio apparente.
Il rilascio del core dalla microcapsula può avvenire con diversi meccanismi di rilascio: per diffusione, degradazione, contatto con solvente o variazioni di pH, temperatura e pressione. Se, come materiale di rivestimento, viene utilizzata una combinazione di polimeri, più̀ di un meccanismo di rilascio reagirà̀ sulle capsule in questione.
Tecniche di microincapsulazione
Nella scelta del metodo di microincapsulazione, le proprietà fisiche e chimiche del nucleo e del materiale di rivestimento e la posizione del componente alimentare da rivestire, hanno un’importanza significativa (Koç et al., 2015). Le microcapsule possono essere ottenute attraverso metodi differenti; la scelta del processo da applicare dipende strettamente da diversi fattori, quali:
- natura del materiale da incapsulare (core): lo stato fisico (solido o liquido), idrofilia/lipofilia, stabilità termica o pH dipendente;
- natura del mezzo di incapsulazione: solventi organici o acquosi, gas;
- struttura delle microparticelle da ottenere: microsfere o microcapsule;
- motivazioni economiche: rapporto costo/qualità, esistenza di brevetti (Koç et al., 2015; Poshadri e Aparna, 2010).
Tra le tecniche più diffuse lo spray dryer, lo spray cooling, i metodi di estrusione, l’emulsificazione, il rivestimento a letto fluido e la coacervazione.
Tutte le metodiche prevedono degli step comuni: dispersione del core in un opportuno solvente; aggiunta del materiale polimerico dello shell; cross-linking dello shell attorno al core; stabilizzazione chimico-fisica delle microcapsule.
Spray-drying
Lo spray drying è una delle prime tecnologie implementate per la microincapsulazione, ancora ampiamente utilizzata. Viene spesso impiegata nell’industria alimentare (sono circa il 90% le microcapsule preparate con questa tecnica) per il suo basso costo e poiché, rispetto alle altre tecniche convenzionali, offre il vantaggio interessante di produrre microcapsule in un’operazione di elaborazione continua relativamente semplice. Core e shell vengono disciolti in un opportuno solvente e omogeneizzati; la miscela è successivamente immessa in uno spray dryer ed atomizzata mediante un ugello all’interno di una camera di essiccazione; a contatto con l’aria calda il solvente evapora e le capsule si raccolgono sul fondo dello spray-dryer. Durante questo processo di essiccazione, l’evaporazione del solvente, che è molto spesso acqua, è rapida e l’intrappolamento del composto di interesse avviene quasi istantaneamente (Fig.3a) (Gharsallaoui et al., 2007). Gli apparecchi con cui viene effettuata questa tipologia di microincapsulazione sono detti spray-dryer, o nebulizzatori, e ne esistono di diversi modelli, ma in tutti sono presenti le seguenti parti principali: ugello di nebulizzazione, sistema di riscaldamento dell’aria, camera di essiccamento, ventilatore, ciclone, recipiente di raccolta del prodotto solido ottenuto (Fig.3b).
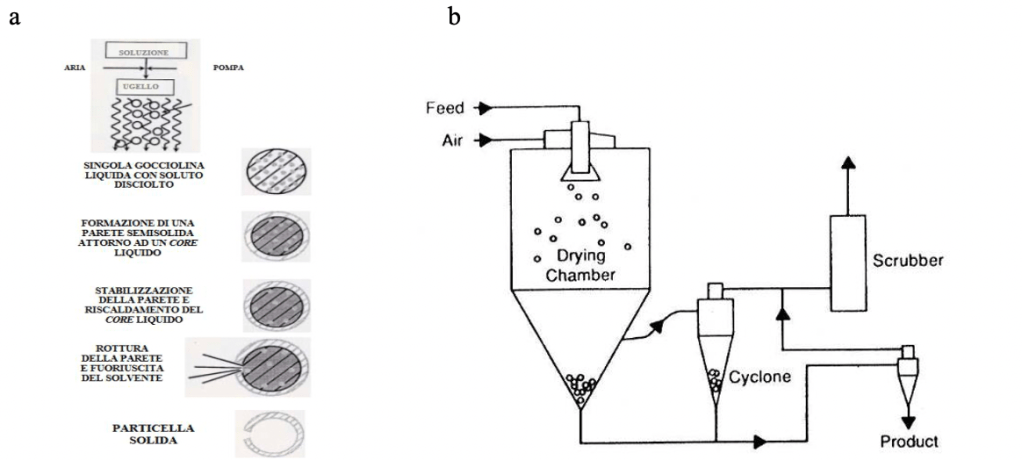
Nel caso in cui la soluzione contenga solvente organico, e non acqua, esistono spray-dryer dotati di trappola per far sì che i fumi dell’evaporazione non vengano dispersi nel locale adibito all’essiccazione. Più frequentemente, gli spray-dryer vengono alimentati con dispersioni a base d’acqua; questo è considerato uno svantaggio poiché la scelta dei materiali di rivestimento risulta essere più limitata. Si utilizzano prevalentemente amido, maltodestrine e gomme, per la loro alta solubilità. Possono essere incapsulati ingredienti alimentari come oli, aromi e antiossidanti. Le capsule che si ottengono sono polinucleari o di tipo a matrice; hanno una buona qualità, sono di piccole dimensioni, con un’alta stabilità e a rapida dissoluzione.
Spray cooling
Lo spray cooling, o raffreddamento a spruzzo, è tipicamente utilizzato per incapsulare sostanze idrofile, come vitamine o minerali, all’interno di uno shell di natura idrofobica. All’interno di una camera avviene l’atomizzazione, per mezzo di un ugello, della soluzione di alimentazione contenente il composto bioattivo ed il polimero di rivestimento. Sempre all’interno della camera si ha la nebulizzazione di un flusso di aria, o azoto liquido, che entra in contatto con la soluzione preparata e permette la solidificazione delle particelle, che saranno caratterizzate da una forma sferica molto regolare (Risch, 1995).
Estrusione
Il processo di estrusione consiste nel far cadere delle gocce di una soluzione acquosa, contenete l’ingrediente funzionale e il polimero di rivestimento (tipicamente alginato di sodio), in un bagno di gelificazione (tipicamente calcio cloruro) (Krasaekoopt, 2003). Tecnologia semplice ed economica che non richiede un forte investimento iniziale in quanto lo strumento necessario per il procedimento può essere semplicemente una pipetta, una siringa, un ugello vibrante o uno “jet cutter”.
Rivestimento a letto fluido
Tra le metodologie più dispendiose, il rivestimento a letto fluido: prevede che le particelle solide del core siano sospese in un flusso d’aria ad una specifica temperatura all’interno di una camera; la copertura avviene mediate l’atomizzazione e la nebulizzazione dello shell, tipicamente costituito da derivati di cellulosa, amido o proteine, direttamente sul core (Dewettinck e Huyghebaert, 1999). Questo processo è spesso utilizzato per aggiungere un rivestimento secondario, in modo tale da migliorare la protezione delle molecole attive nel nucleo.
Esistono diverse tecniche di rivestimento a letto fluido (Fig.5):
- nebulizzazione dall’alto;
- processo Wurster;
- letto fluido rotante;
- deposizione elettrostatica (Gouin, 2004).

Coacervazione
La coacervazione è il processo fisico di separazione di fase e consiste di tre step, tutti svolti sotto costante agitazione.
Inizialmente è prevista la formazione di una soluzione composta da: nucleo, materiale di rivestimento e solvente (Tolve et al., 2016); solo a questo punto è possibile indurre la coacervazione del sistema. Si può agire in modo differente:
- variando la temperatura: sfrutta la diversa solubilità del polimero a varie temperature;
- variando il pH: sfrutta la diversa solubilità del polimero a vari pH;
- aggiungendo sali: il sale sottrae acqua al polimero facendolo coacervare e poi precipitare (salting out);
- aggiungendo un non solvente: si aggiunge alla miscela (solvente + polimero) un solvente miscibile con il solvente usato per sciogliere il polimero ma nel quale il polimero è insolubile;
- addizionando un polimero incompatibile: si basa sull’aggiunta di un polimero incompatibile a quello che formerà la membrana. I due polimeri sono disciolti nello stesso solvente. Mescolando le soluzioni dei due polimeri, uno di questi coacerva. Di conseguenza solo un polimero formerà la membrana;
- tramite coacervazione complessa: si utilizzano due polimeri, uno anionico e uno cationico, che reagiscono formando un complesso che si separa dalla soluzione. Entrambi i polimeri saranno parte dello shell.
Si formano così due fasi: una che è ricca di polimeri (coacervati) e un’altra principalmente costituita del solvente.
La seconda fase comprende la deposizione del polimero liquido sul materiale del nucleo e nella terza fase lo strato di rivestimento viene solidificato attraverso raffreddamento, desolvatazione o reticolazione, in modo da ottenere una membrana rigida e resistente attorno alle particelle del core sospeso (Tolve et al., 2016). Le microparticelle si recuperano poi per filtrazione.Un gran numero di materiali di rivestimento è stato valutato per l’applicazione della coacervazione, ma il sistema più comune è costituito da una miscela di gelatina e gomma di acacia che è stato utilizzato, ad esempio, per la microincapsulazione di olio di semi di papavero (Poshadri e Aparna, 2010).
Bibliografia
- Al-Mosawi, A.J., Thevenet F. Acacia gum (gum arabic). Blackwell Publishing; 2006.
- Chan, E. S., Lee, B. B., Ravindra, P., & Poncelet, D. (2009). Prediction models for shape and size of ca-alginate macrobeads produced through extrusion–dripping method. Journal of colloid and interface science, 338(1), 63-72.
- Dewettinck, K., & Huyghebaert, A. (1999). Fluidized bed coating in food technology. Trends in Food Science & Technology, 10(4-5), 163-168.
- Dziezak JD (1988): Microencapsulation and encapsulated food ingredients. Food Technology 42, 136±151.
- Gharsallaoui, A., Roudaut, G., Chambin, O., Voilley, A., & Saurel, R. (2007). Applications of spray-drying in microencapsulation of food ingredients: An overview. Food research international, 40(9), 1107-1121.
- Koç, M., Güngör, Ö., Zungur, A., Yalçın, B., Selek, İ., Ertekin, F. K., & Ötles, S. (2015). Microencapsulation of extra virgin olive oil by spray drying: effect of wall materials composition, process conditions, and emulsification method. Food and bioprocess technology, 8(2), 301-318.
- Krasaekoopt, W., Bhandari, B., & Deeth, H. (2003). Evaluation of encapsulation techniques of probiotics for yoghurt. International dairy journal, 13(1), 3-13.
- Poshadri, A., & Aparna, K. (2010). Microencapsulation technology: a review. Journal of Research ANGRAU, 38(1), 86-102.
- Putnam, D. E., & Garrett, J. E. (2005). Microencapsulation opportunities to improve animal products and nutrition. In Proceedings.
- Risch, S. J. (1995). Encapsulation: overview of uses and techniques.
- Silva, P. T. D., Fries, L. L. M., Menezes, C. R. D., Holkem, A. T., Schwan, C. L., Wigmann, É. F., … & Silva, C. D. B. D. (2014). Microencapsulation: concepts, mechanisms, methods and some applications in food technology. Ciência Rural, 44(7), 1304-1311.
- Temiz, U., & Öztürk, E. (2018). Encapsulation methods and use in animal nutrition. Selcuk Journal of Agriculture and Food Sciences, 32(3), 624-631.
- Tolve, R., Galgano, F., Caruso, M. C., Tchuenbou-Magaia, F. L., Condelli, N., Favati, F., & Zhang, Z. (2016). Encapsulation of health-promoting ingredients: applications in foodstuffs. International journal of food sciences and nutrition, 67(8), 888-918.
Roberta Tolve, Nicola Condelli, Marisa C. Caruso, Fernanda Galgano
Contatti: fernanda.galgano@unibas.it
